Vahulaike veepinnal või vahuseid laineharjasid on meist igaüks näinud. Kahetsusväärselt tihti seostub aga vahutav vesi meie jaoks reostuse või lihtsalt veekogu kehva seisundiga. Küll on järvevee vahule ajanud sinna sattunud pesuvahendid või arvatakse ojas voolavat naabrimehe saunavesi. Loodusvetele loomulikuks nähtuseks peetake vahtu pigem harva. Möödunud kevadel pöördus üks asjalik Viljandimaa keskkonnaametnik minu poole abipalvega, kuidas valvsale kodanikule seletada ühel Navesti jõe lõigul esinevat öist või varahommikust vee vahutamist. Talle saadetud vastuse panin nüüd pikemalt kirja.
Keemikute keeles on vaht pihus ehk pihussüsteem, kus suhteliselt väikesesse vedelikukogusesse on pihustunud rohkelt gaasi. Vaht tekib vedelikus hõljuvatest gaasimullidest ja vahu iseloomu määravad mulle eraldava vedelikukile keemiline koostis ja füüsikalised omadused. Seega on vahu tekkimiseks vajalik gaasimullide allikas, mis toodab mulle kiiremini, kui need kaduda jõuavad. Loodusvetes on üheks mullide moodustajaks vee keeriseline voolamine, mille abil segatakse õhk vette. Nõnda tekitavad mullid murdlainetuse korral, kärestikes või paisude järel.

Mullid võivad olla ka mingi keemilise reaktsiooni tulemus. Näiteks järvesette biokeemilisel lagunemisel moodustuvad süsihappegaasi ja metaanimullid. Peale tekkimist hakkavad mullid kiirelt muutuma. Gaas difundeerub väiksematest mullidest suurematesse ning mullid hakkavad kasvama. Kui mull saavutab piisavalt suure ruumala, tõuseb see tänu üleslükkejõule veepinnale ning moodustab koos teiste mullidega vahu.
Täiesti puhas vesi ei vahuta. Veepinnale jõudvad gaasimullid purunevad kohe, kui neid ümbritsev vedelikukile raskusjõu mõjul laiali valgub. Voolamine ja aurustumine ongi mullide suurimad vaenlased. Suletud pudelis lisanditeta vee raputamisel moodustuvad vähesed mullid vaid mõneks hetkeks. Vahu teke ja püsivus on suuresti seotud pindpinevusega. Vedelas vees on iga molekul ümbritsetud ühtlaselt naabermolekulidega ja seotud kohesioonijõududega. Viimased on keskmiselt võttes tasakaalus. Veest väljaspool leidub (gaasi)molekule väga vähe ja taolist tasakaalu tekkida ei saa. Seetõttu mõjub vee pinnakihi molekulidele summaarne tõmme vedeliku sisemuse suunas ning vedeliku pinnakihis kujuneb teatav pinge. Vee ja õhu piirpind on alati võimalikult väike ning antud ruumala juures on minimaalne pind keral ja muude jõudude puudumisel on vedelikupiisk alati kerakujuline. Seda nähtust nimetatakse pindpinevuseks. Et vältida mulli moodustava vedelikukile muutumist tilkadeks, peab vees leiduma pindpinevust vähendavaid nn pindaktiivseid aineid. Nende molekulid koosnevad hüdrofiilsest (veelembene) ja hüdrofoobsest (vett hülgav) osast.
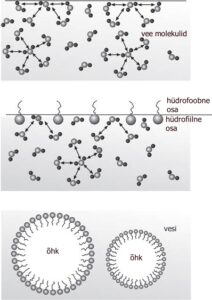
Selliste molekulide hüdrofiilne osa moodustab sideme veemolekulidega, takistades veemolekulide omavahelist seondumist ja vähendades pindpinevust. Pindpinevuse vähenemisel pääseb õhk kergemini vette ja võimalus mulle moodustada on suurem. Pindaktiivsete ainete molekulid ja veemolekulid moodustavad omalaadse elektrilise kaksikkihi, mis takistab vedelikukile rebenemist ja suurendab mulli eluiga. Mullide puhul on veel oluline, et kilet moodustav vedelik oleks piisavalt viskoosne ja ei voolaks kiiresti pindade vahelt ära.
Looduslikke pindaktiivseid aineid leidub veekogudes üksjagu. Neist peamise osa moodustab taimse päritoluga lahustunud orgaaniline aine, mis võib pärineda mullast või veekogust endast. Rohkelt leidub seda humiinainetena näiteks rabajärvedes ning lipiidide ja proteiinidena veekogudes, kus toimuvad planktonvetikate õitsengud või kasvab arvukalt veetaimi. Anorgaaniliste ainete mõju pindpinevusele on erinev. Reeglina on soolalahuste pindpinevus puhta vee omast suurem. Happed aga vastupidi vähendavad pindpinevust ning samamoodi toimivad ka nõrkade hapete soolad, sest nende hüdrolüüsil tekivad happed. Teisalt on peamiselt kuivas kliimavöötmes leiduvate soodajärvede vesi väga aluseline ning kaldad ikkagi vahused. Neis järvedes on rohkesti lahustunud naatriumkarbonaati, mis kuulub oma hea seebistamisvõime tõttu detergentide hulka. Kare vesi (sisaldab rohkelt kaltsiumi- ja magneesiumiioone) pärsib vahu teket, sest karedust põhjustavad positiivsed ioonid seonduvad negatiivselt laetud pindaktiivsete ainete molekulidega. Seepärast vahutavad paremini pehme veega vähetoitelised järved kui peamiselt põhjaveest toituvad vooluveekogud.

Pindpinevus väheneb samuti veetemperatuuri tõustes. Siiski on vesikeskkond termiliselt üsna stabiilne ja ööpäevastel temperatuurikõikumistel märgatavat mõju vahu tekkimisele või kadumisele pole. Pigem laguneb soojemal aastaajal valgala orgaaniline aine hõlpsamalt ning rikastab sellega veekogusid.
Kui veekogu vahutab, siis ei tasuks kohe tormata süüdlast otsima, vaid enne tuleks vahtu lähemalt uurida. Looduslik vaht võib levida laial alal ning koguneda vettelangenud puude taha või kuhjuda tuulepealsetel kallastel lausa vallideks. Suuremate veekogude avavees võib pinnalainetus moodustada omalaadsed rööpsed vahuvöödid. Looduslikku vahu mullid on suured ning vaht hajub võrdlemisi kiiresti. Oma tekkemomendil võib see olla valge aga värvub lahustunud orgaanilise aine tõttu aja jooksul kollakaks või pruunikaks. Tulvaveega tekib rohke heljumi tõttu üsnagi räpase välimusega vahukiht. Looduslikule vahule on iseloomulik pinnase-, rohu- või isegi kalalõhn. Selline vaht on tervisele üldiselt kahjutu, sest pindaktiivseid ained leidub seal ligikaudu protsendi jagu ning ülejäänud osa moodustavad õhk ja vesi. Suhu toppida seda siiski ei maksa. Me ei joo ju keetmata jõe- ja järvevett. Lisaks võib vaht olla rikastatud erinevate hüdrofoobsete ainetega nagu raskmetallid või kloororgaanilised ühendid.
Sünteetiliste pindaktiivsete ainete poolt tekitatud vaht on pigem väikeste mullidega ja tihedam. Katsudes on see tuntavalt libe või isegi kleepuv. Levib eelkõige reostusallika lähistel ning allika kadumisel kaob ka vaht ja selle tekkimist ei saa seostada tuule või tulvavetega. Värvuselt on see erkvalge või siis sootuks ebatavalise tooniga. Lõhnas on tajutavad erinevad olmekemikaalid ja parfüümid või hoopis roiskumisele ja käärimisele omased aroomid.
